Spectrométrie (HU) : Différence entre versions
| Ligne 24 : | Ligne 24 : | ||
| − | <center><math>A | + | <center><math>A = ε.l.C</math></center> |
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
Avec : | Avec : | ||
| Ligne 37 : | Ligne 32 : | ||
===Schéma de principe d'un spectromètre=== | ===Schéma de principe d'un spectromètre=== | ||
| + | |||
[[File:spectromètre.JPG|400px|center|thumb|<center>''<u>Source</u> : [https://fr.wikipedia.org/wiki/Spectrophotom%C3%A9trie Article Wikipédia].''</center>]] | [[File:spectromètre.JPG|400px|center|thumb|<center>''<u>Source</u> : [https://fr.wikipedia.org/wiki/Spectrophotom%C3%A9trie Article Wikipédia].''</center>]] | ||
Version du 20 avril 2020 à 14:25
Traduction anglaise : Spectrometry
Dernière mise à jour : 20/4/2020
Méthode analytique qui consiste à mesurer l'absorbance d'une substance chimique donnée, généralement en solution.
Principe de la spectrométrie
Le principe du dosage spectrométrique d'une substance consiste à utiliser la relation existant entre l'absorbance de la solution et la concentration de la substance étudiée.
Loi de Beer-Lambert
On définit l'absorbance $ A_λ $ d'une solution pour la longueur d'onde $ λ $ par la relation (1) :
Avec :
- $ I_0 $ : intensité du faisceau incident pour la longueur d'onde λ ;
- $ I $ : intensité transmise pour la longueur d'onde.
La loi de Beer-Lambert permet de relier cette absorbance à la concentration :
Avec :
- $ ε_λ $ : coefficient d'extinction molaire pour la longueur d'onde λ (litres/mole/m) ;
- $ l $ : longueur traversée par le faisceau incident (m) ;
- $ C $ : concentration de la solution (moles/Litre).
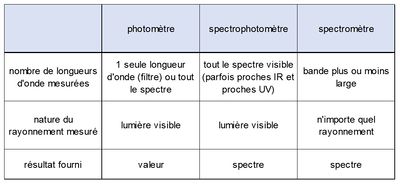
Schéma de principe d'un spectromètre
La loi de Beer-Lambert reste linéaire pour des concentrations $ C $ peu élevées, et la lecture de l'intensité transmise $ I $ donne directement la concentration C après étalonnage de l'appareil. Cette méthode est très fréquemment utilisée pour déterminer les concentrations de certains polluants dans les eaux, par exemple les nitrates (norme AFNOR NF T 90-012) et les orthophosphates (norme AFNOR NF T 90-023).
 S'abonner à un flux RSS
S'abonner à un flux RSS