Cycle de l’azote (HU) : Différence entre versions
| Ligne 1 : | Ligne 1 : | ||
''<u>Traduction anglaise</u> : Nitrogen cycle'' | ''<u>Traduction anglaise</u> : Nitrogen cycle'' | ||
| − | Ensemble des transformations que peut subir [[Azote (HU)|l'azote]] entre ses | + | Ensemble des transformations que peut subir [[Azote (HU)|l'azote]] entre ses différentes formes physico-chimiques. |
| − | différentes formes physico-chimiques | + | |
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| + | Le cycle de l'azote est complexe car il existe de nombreuses possibilités d'évolution d'une forme donnée vers une autre forme. Nous ne intéresserons qu'à la partie du cycle de l'azote qui se produit principalement dans les milieux aquatiques. Il peut être représenté de façon schématique par la ''figure 1''. | ||
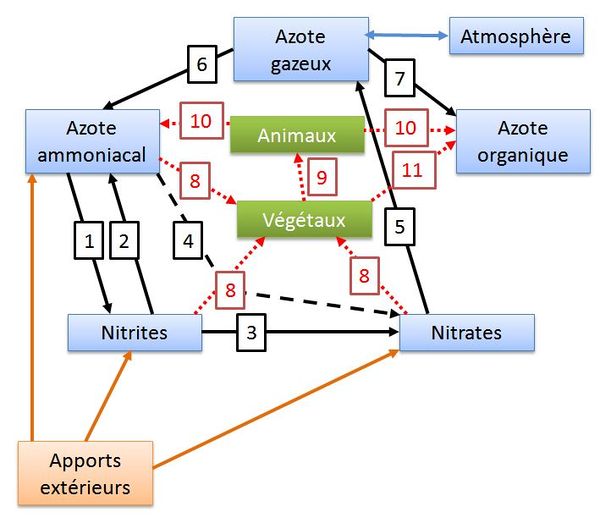
| − | <center> | + | [[File:cycle azote.JPG|600px|center|thumb|<center>''<u>Figure 1</u> : Schéma simplifié du cycle de l'azote : 1 : nitritation ; 2 : nitrosation ; 3 : nitratation ; 4 : nitrification ; 5 : dénitrification ; 6 : ammonification ; 7 : fixation ; 8 : assimilation.''</center>]] |
| + | Les principales transformations représentées sur ce schéma sont les suivantes : | ||
| + | * (1) : <u>nitritation</u> : | ||
| + | * (2) : <u>nitrosation</u> : | ||
| + | * (3) : <u>nitratation</u> : | ||
| + | * (4) : <u>nitrification</u> : | ||
| + | * (5) : <u>dénitrification</u> : | ||
| + | * (6) : <u>ammonification</u> : | ||
| + | * (7) : <u>Fixation de l'azote gazeux</u> : l'azote gazeux, très abondant dans l'atmosphère, est également présent de façon importante dans les milieux aquatiques du fait des échanges permanents entre l'eau et l'air. Il n'est cependant que peu accessible sous cette forme pour la plupart des organismes vivants. Seules les [[Cyanophycée (HU)|cyanophycées]] et certaines plantes légumineuses sont capables de le fixer directement pour le transformer en ion ammonium (<math>NH_4^{+}</math>). Cette fixation (1) peut devenir importante dans les milieux [[Eutrophe (HU)|eutrophes]]. | ||
| + | * (8) :<u>assimilation</u> : | ||
| + | * (9) :<u>absorption</u> : | ||
| + | * (10) :<u>excrétion</u> : | ||
| − | + | Les [[Nitrite (HU)|nitrites]] se transforment en azote gazeux ([[Dénitrification (HU)|dénitrification]]), en [[Nitrate (HU)|nitrate]] ([[Nikuradse Ivan (1894-1979) (HU)|nitratation]]) ou en [[Ammonium (HU)|ammonium]] ([[Nitrosation (HU)|nitrosation]]) en fonction du pH et de la quantité [[Oxygène dissous / OD (HU)|d'oxygène dissous]] disponible. Les ions ammonium sont principalement produits par les excrétions des animaux aquatiques, la décomposition de la matière organique par des bactéries ou des champignons (ammonification) et les apports extérieurs, notamment d'eaux usées domestiques ou de lisiers. Ils peuvent être assimilés directement par certains organismes ou oxydés rapidement si l'eau est bien oxygénée. L'ammonium peut cependant être localement abondant dans les milieux eutrophes ou à proximité des rejets. Dans ce cas, sa concentration peut devenir dangereuse pour les organismes vivants. Il semble également qu'une concentration élevée en ammonium aggrave les conséquences des [[Choc anoxique (HU)|chocs anoxiques]]. | |
| − | + | ||
| − | + | Pour une élimination biologique complète de l’azote contenu dans l’eau, la nitrification doit être suivie d’une deuxième phase : la [[Dénitrification (HU)|dénitrification]]. La nitrification se produit également de manière naturelle dans les cours d’eau et dans les sols. | |
[[Catégorie:Dictionnaire_DEHUA]] | [[Catégorie:Dictionnaire_DEHUA]] | ||
Version du 22 avril 2020 à 17:47
Traduction anglaise : Nitrogen cycle
Ensemble des transformations que peut subir l'azote entre ses différentes formes physico-chimiques.
Le cycle de l'azote est complexe car il existe de nombreuses possibilités d'évolution d'une forme donnée vers une autre forme. Nous ne intéresserons qu'à la partie du cycle de l'azote qui se produit principalement dans les milieux aquatiques. Il peut être représenté de façon schématique par la figure 1.
Les principales transformations représentées sur ce schéma sont les suivantes :
- (1) : nitritation :
- (2) : nitrosation :
- (3) : nitratation :
- (4) : nitrification :
- (5) : dénitrification :
- (6) : ammonification :
- (7) : Fixation de l'azote gazeux : l'azote gazeux, très abondant dans l'atmosphère, est également présent de façon importante dans les milieux aquatiques du fait des échanges permanents entre l'eau et l'air. Il n'est cependant que peu accessible sous cette forme pour la plupart des organismes vivants. Seules les cyanophycées et certaines plantes légumineuses sont capables de le fixer directement pour le transformer en ion ammonium ($ NH_4^{+} $). Cette fixation (1) peut devenir importante dans les milieux eutrophes.
- (8) :assimilation :
- (9) :absorption :
- (10) :excrétion :
Les nitrites se transforment en azote gazeux (dénitrification), en nitrate (nitratation) ou en ammonium (nitrosation) en fonction du pH et de la quantité d'oxygène dissous disponible. Les ions ammonium sont principalement produits par les excrétions des animaux aquatiques, la décomposition de la matière organique par des bactéries ou des champignons (ammonification) et les apports extérieurs, notamment d'eaux usées domestiques ou de lisiers. Ils peuvent être assimilés directement par certains organismes ou oxydés rapidement si l'eau est bien oxygénée. L'ammonium peut cependant être localement abondant dans les milieux eutrophes ou à proximité des rejets. Dans ce cas, sa concentration peut devenir dangereuse pour les organismes vivants. Il semble également qu'une concentration élevée en ammonium aggrave les conséquences des chocs anoxiques.
Pour une élimination biologique complète de l’azote contenu dans l’eau, la nitrification doit être suivie d’une deuxième phase : la dénitrification. La nitrification se produit également de manière naturelle dans les cours d’eau et dans les sols.
 S'abonner à un flux RSS
S'abonner à un flux RSS